Having never forgot how original I felt when, in the early 1980's, I took my micropaleontology course and then prepared a short dissertation about benthic foraminiferans from Middle Pliocene, I harbored for more than 30 years the intention of getting in touch again with those small incredible organisms.
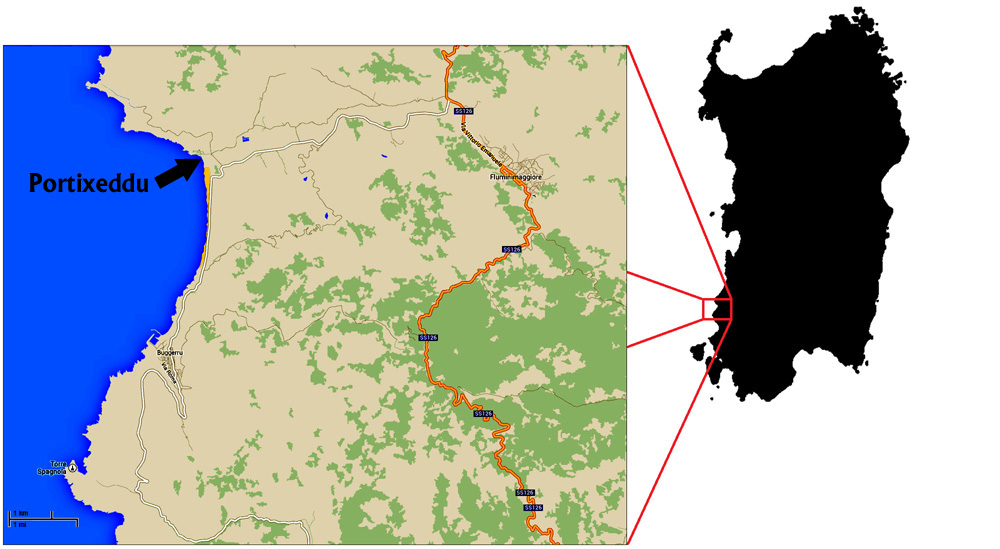
Easier said than done: anybody dealing with this subject knows well how painstaking and time consuming this pastime can be. In my case, a small scoop of Sardinian sand (well, a few well chosen small scoops!) that I collected in 2015, translated into more than two years of very discontinuous activity.
Still, after buying an used stereomicroscope, selecting by hand the foraminiferans from the sand, buying an eyepiece adapter for my venerable Sony A230 camera, I was stuck - I couldn't find the few days needed to select, glue, photograph and determine the specimens.
Then August 2017 came, with a long period of vacation, again in Sardinia, my favorite location: and I got everything with me (even the foraminiferans, back to their homeland!), microscope, camera, brushes, slides, glue and new 5x eyepieces that meant less headaches and dizziness even after hours of use - but I still didn't know, I was resigned to do the work 20 minutes a day.
And so I did it: herein above you'll find the links to two photos of as many multi-cell slides. Each cell in each slide is linked to an half size preview of a picture: please excuse me for the poor quality, but around 900px per millimeter is what my outdated photographic setup allows for now. Despite focus stacking (see below) the pictures are quite soft and blurred, as can be expected when the camera is detached from the objective and diaphragm control is unavailable, but the species should be recognizable in any case.
I thank Michael Hesemann of foraminifera.eu for his precious help and generous advice. As stated under each photo, I, Cesare Brizio, bring full responsibility for any misidentification of the species.
Non avendo mai dimenticato quanto originale mi sono sentito quando, nei primi anni '80, ho frequentato il corso di micropaleontologia e poi ho preparato una tesina sui Foraminiferi bentonici del Pliocene Medio, ho coltivato per più di 30 anni l'intenzione di tornare in contatto con questi piccoli incredibili organismi.
Più facile a dirsi che a farsi: chiunque si occupi di questo argomento sa bene quanto tempo e attenzione richieda questo passatempo. Nel mio caso, una piccola cucchiaiata di sabbia sarda (beh, alcune piccole cucchiaiate ben scelte!) raccolte nel 2015, si sono tradotte in più di due anni di attività molto discontinua.
Tuttavia, dopo aver acquistato un stereomicroscopio usato, scegliendo manualmente i Foraminiferi dalla sabbia, acquistando un adattatore per oculare per la vetusta fotocamera Sony A230, sono rimasto bloccato - non ho trovato i pochi giorni necessari per selezionare, incollare, fotografare e determinare gli esemplari.
Poi è arrivato l'Agosto del 2017, con un lungo periodo di vacanza, di nuovo in Sardegna, il mio posto preferito: e ho portato tutto con me (anche i Foraminiferi, tornati in patria!), microscopio, fotocamera, pennelli, vetrini, colla e nuovi oculari 5x che hanno voluto dire meno emicranie e vertigini anche dopo ore di utilizzo - ma ancora non lo sapevo, ero disponibile a fare il lavoro 20 minuti al giorno.
E così ce l'ho fatta: qui sopra, due link a due foto di altrettanti vetrini multi-cella. Ogni cella di ciascun vetrino è collegata ad un'anteprima di mezza dimensione di un'immagine: per favore scusate la scarsa qualità, ma circa 900px per millimetro è ciò che la mia attrezzatura fotografica obsoleta consente attualmente. Nonostante il focus stacking (vedi sotto) le immagini sono abbastanza morbide e sfocate, come ci si può aspettare quando la fotocamera è staccata dall'obiettivo e il controllo del diaframma non è disponibile, ma la specie dovrebbe essere riconoscibile in ogni caso.
Ringrazio Michael Hesemann di foraminifera.eu per il suo aiuto prezioso e dei generosi consigli. Come indicato sotto ogni foto, io, Cesare Brizio, ho la piena responsabilità per ogni errata identificazione delle specie.
I selected the specimens manually from the sand, with a brush, using a Bresser Researcher ICD stereomicroscope under low magnification (20x). The microscope has stereo objectives capable of 2x and 4x magnification, and was provided with 10x and 20x WF eyepieces.
Slide preparation (glueing and positioning) was performed at even lower magnification (10x) thanks to 5x eyepieces that I bought separately.
Ho selezionato gli esemplari manualmente dalla sabbia, con un pennello, utilizzando uno stereomicroscopio Bresser Researcher ICD a basso ingrandimento (20x). Il microscopio è dotato di obiettivi stereo 2x e 4x e dotato di oculari WF da 10x e 20x WF.
La preparazione dei vetrini (incollaggio e posizionamento) è stata effettuata con ingrandimento ancora minore (10x) grazie a oculari da 5x che ho acquistato separatamente.
Slides were photographed with a Sony Alpha A230 DSLR camera, with a 10Mpx sensor, using the classic autofocus objective Sony 3.5-5.6/18-55 SAM (at the time, sold in bundle with the camera), with the interposition of a 13mm extension tube.
Two photos (single shot, no focus stacking) were taken for each slide, and were manually juxtaposed (as a consequence, a vertical junction line can be observed in the pictures).
I vetrini sono stati fotografati con una fotocamera DSLR Sony Alpha A230, con sensore da 10Mpx, utilizzando il classico obiettivo Sony 3.5-5.6 / 18-55 SAM (a suo tempo venduto in bundle con la fotocamera), con l'interposizione di un tubo di prolunga di 13 mm. Due foto (singolo scatto, senza focus stacking) sono state scattate per ciascun vetrino e sono state giustapposte manualmente (di conseguenza, una linea di giunzione verticale può essere osservata nelle immagini).
I have the intention to get better pictures of each specimen in the months that will follow, thanks to another monocular microscope of mine. For now, I decided to photograph the specimens with the very same stereomicroscope that I used to select the specimens and prepare the slides.
Please understand that I do perfectly know that such a setup is "suboptimal" at best.
Ho l'intenzione di ottenere immagini migliori di ciascun campione nei mesi che seguiranno, grazie ad un altro microscopio monoculare. Per ora ho deciso di fotografare gli esemplari con lo stesso stereomicroscopio che ho usato per selezionarli e preparare i vetrini.
Si prega di capire che so perfettamente che una tale impostazione è, per usare un eufemismo, "subottimale".
Thus, provisionally, single foraminiferans were photographed with the Sony Alpha A230 DSLR camera body, attached to a Bresser T2 30mm eyepiece adapter, placed in one of the binocular tubes of the Bresser microscope.
To overcome the minimal depth of field, from three (smallest specimens) to seven (biggest specimens) pictures of each specimen were taken with slight increases of the focusing distance, with the limitation of a coarse-focus-only column. As long as the stereomicroscope head wasn't trinocular, with the camera mounted at an eyepiece station, parallax shift occurred between the pictures of each specimen.
As seen from the DSLR camera eyepiece, the view field was very dark: the microscope built-in reflected light illuminator, whose original halogen bulb was substituted with a dimmable 140 lumen H4 LED bulb, was complemented by a desk lamp mounting a 5W natural light LED bulb, suitably positioned to avoid shadows.
The camera was set in manual mode and shots were taken at ISO 200, 1/4 of a second exposure time, using the 4x objective, that allowed a field of view of around 4mm x 3mm with almost no vignetting.
To improve steadiness, shooting was commanded by an IR remote switch.
Pictures were Z-stacked by Helicon Focus 6 Lite software, that managed well the parallax shift, improving picture quality, but that couldn'to miracles: in particular, the "dust map" function wasn't available in this version, and dust specks in the objective or in the prism appeared repeatedly in the composite image, requiring some "photoshopping".
Così, provvisoriamente, i singoli Foraminiferi singoli sono stati fotografati con il corpo telecamera Sony Alpha A230 DSLR, collegato ad un adattatore T2 Bresser per oculare da 30mm, posizionato in uno dei tubi oculari del microscopio Bresser.
Per superare la modestissima profondità di campo, per ciascun esemplare sono stati realizzati da tre (esemplari più piccoli) a sette (esemplari più grandi) scatti, ripresi con lievi incrementi della distanza di messa a fuoco, nei limiti di un corpo microscopio non dotato di regolazione fine. Dato che la testa dello stereomicroscopio non era trinoculare, con la fotocamera montata al posto di un oculare, si è verificato un cambio di parallasse tra i singoli scatti di ciascun campione.
Come visto dall'oculare della fotocamera DSLR, il campo visivo era molto scuro: l'illuminatore a luce riflessa incorporato nel microscopio, la cui lampadina alogena originale è stata sostituita da una lampadina H4 LED da 140 lumen dimmerabile, è stato complementato da una lampada da tavolo dotata di bulbo LED da 5W a luce naturale, opportunamente posizionata per evitare le ombre.
La fotocamera è stata impostata in modalità manuale e gli scatti sono stati presi a ISO 200, 1/4 di secondo di esposizione, utilizzando l'obiettivo 4x, che ha consentito un campo visivo di circa 4mm x 3mm con quasi nessuna vignettatura.
Per migliorare la stabilità, lo scatto è stato comandato da un interruttore IR remoto.
Le immagini di ciascun esemplare sono state impilate col software Helicon Focus 6 Lite, che ha gestito bene lo spostamento di parallasse, migliorando la qualità dell'immagine, ma che non ha potuto fare miracoli: in particolare, la funzione "mappa della polvere" non era disponibile in questa versione, e granelli di polvere nell'obiettivo o nel prisma sono apparsi ripetutamente nell'immagine composita, richiedendo alcuni interventi con Photoshop.
Slides were provided by www.microslides.kreativika.sk.
To store the specimens, I initially did the stupid choice to select the "deep well" slides, but a deep well means shadows and makes difficult to recovery the specimen from the "black depths".
On the other side, wide, multi-cell slides are great!
Overall, I'm satisfied with their price/quality ratio, but please be advised that, unless Kreativika recently changed its quality standards, a great number of black particles may appear as soon as a drop of water gets in touch with the slides, in particular of the pit walls.
I don't know whether they are carbonized residues of the laser cut, or traces of toner: I suggest to vacuum clean them carefully, and also to pass a wet brush (not the one that you'll use for the foraminiferans!!!) around all the borders before using the slides.
I vetrini sono stati forniti da www.microslides.kreativika.sk.
Per conservare gli esemplari, ho inizialmente fatto la scelta stupida di selezionare vetrini "profondi", ma pozzetti profondi vogliono dire ombre, e rendono difficile il recupero del campione dalle "oscure profondità".
D'altra parte, i vetrini ampi e multi-cella sono fantastici! Nel complesso, sono soddisfatto del loro rapporto qualità / prezzo, ma si prega di ricordare che, a meno che Kreativika non abbia recentemente modificato i propri standard qualitativi, un gran numero di particelle nere possono apparire non appena una goccia d'acqua entra in contatto con le diapositive, in particolare col bordo dei pozzetti.
Non so se sono residui carbonizzati del taglio laser o tracce di toner: suggerisco di pulirle attentamente con aspirapolvere e anche di passare un pennello bagnato (non quello che userete per i Foraminiferi!!! ) intorno a tutti i bordi prima di utilizzare i vetrini.
Thirty-five years ago I wasn't particularly good as a foraminiferan manipulator, nor particular proficient in their recognition - so, I can't talk about "lost abilities...." but rather of "abilities that I never had".
The challenge was exactly that: getting a decent result by overcoming my clumsiness. And I'm happy, even though I did a lot of mistakes and any competent person would rise his brow with the result. To cite only my most evident shortcomings:
Thank you for reading so far: I just wanted to share with you this small adventure of mine.
Trentacinque anni fa, non ero particolarmente bravo come manipolatore di Foraminiferi, né particolarmente competente nel loro riconoscimento - quindi non posso parlare di "abilità perdute" ma piuttosto di "abilità mai possedute".
La sfida era esattamente quella: ottenere un risultato decente superando la mia goffaggine. E sono felice, anche se ho commesso molti errori e qualunque persona competente avrebbe da ridire sui risultati. Per citare solo le mie carenze più evidenti:
Grazie per aver letto fin qui: ho solo voluto condividere con voi questa mia piccola avventura.